La maladie de Newcastle (ND) est une maladie virale majeure chez la volaille dans le monde entier. La vaccination reste la principale méthode de contrôle dans les pays endémiques. Diverses stratégies de vaccination, y compris l'utilisation de vaccins recombinants récemment développés ont été utilisées pour le contrôle de la maladie. A ce jour, le Vectormune®ND est le vaccin qui permet d'obtenir les meilleurs résultats dans le contrôle de la maladie de Newcastle chez le poulet, y compris dans des zones fortement infectées.
Vectormune®ND est un vaccin recombinant, utilisant l'herpesvirus de la dinde (HVT) comme vecteur pour exprimer l’antigène clé du virus de la maladie de Newcastle (NDV). Ce vaccin est développé pour éviter les inconvénients liés à l'utilisation des vaccins conventionnels.
En effet, le virus vecteur HVT du Vectormune® ND a des caractéristiques bénéfiques uniques :
- il est extrêmement sûr ;
- il n’interfère pas avec les anticorps d’origine maternelle, et peut donc être appliqué dans le couvoir, soit in ovo, soit chez les poussins d'un jour ;
- Il persiste dans le corps de l'oiseau, ainsi il induit une réponse immunitaire à chaque stimulation conférant ainsi une immunité à vie ;
- Il confère une excellente protection contre les différentes souches de NDV chez le poulet incluant notamment les génotypes des souches sauvages circulant sur le terrain (génotypes II,IV,V,VII et VIII).
Une étude a été réalisée en collaboration avec le département des sciences et techniques de l’Université Ibn Tofail, l’ONSSA au Maroc et Ceva santé Animale, pour tester l'efficacité du Vectormune® ND, vaccin vectorisé, sur virus HVT exprimant le gène F du NDV (rHVT-F) contre le virus du génotype IV de la maladie de Newcastle chez la dinde chair.
L’étude a porté sur des dindes chairs issues de reproducteurs vaccinés contre la maladie de Newcastle et ayant des titres élevés en anticorps maternels (8.7 ±0.8log2titré par IH). Les dindes ont été divisées en deux groupes, un groupe vacciné et un groupe de contrôle. Les dindes ont été vaccinées à un jour dans le couvoir par voie sous-cutanée avec Vectormune® ND.
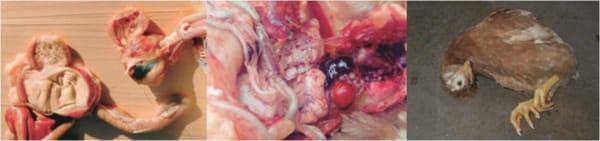
Les deux groupes de dindes ont été challengé par une souche marocaine vélogénique viscerotrope NDV JEL du génotype IV à l’âge de 3 et 4 semaines. Les dindes challengées ont été observées chaque jour pour faire l’évaluation clinique et les mesures de performances. Chez les dindes non vaccinées les signes cliniques ont été observés à 3-5 jours post challenge alors que sur les animaux vaccinés aucun signe clinique n’a été détecté.
L’évaluation de la vaccination a été réalisée par la technique PCR pour la détection du virus vaccinal sur des prélèvements de foie, de follicule plumeux à l’âge de 3 et 4 semaines sur des dindes appartenant au groupe vacciné et au groupe contrôle. Le virus vaccinal a été détecté chez 100 % des dindes vaccinées, dès l'âge de 21 jours au niveau du foie et du follicule plumeux.
L’étude a également révélé une décroissance du gain de poids dans le groupe non vacciné alors que dans le groupe vacciné les performances étaient maintenues.
L'étude a également montré que l’excrétion du virus post challenge par la voie oro-nasale et cloacale est considérablement réduite par la vaccination en comparaison au groupe contrôle.
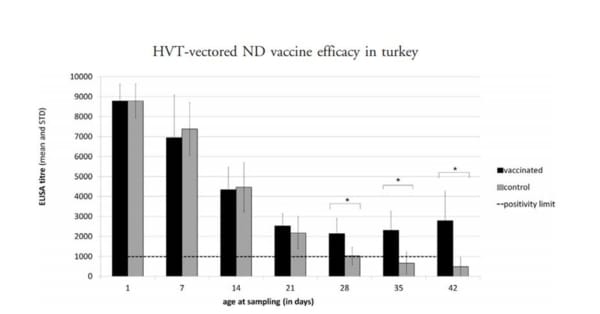
Le développement d'une réponse immunitaire humorale post-vaccinale a été détecté à partir de 4 semaines d’âge par la technique ELISA.
Cette étude montre que les dindes vaccinées avec Vectormune®ND ne présentent pas de signes cliniques et sont protégées contre les infections par des souches NDV velogeniques.
Vectormune®ND, entraîne une réduction de l’excrétion des virus sauvages et permet donc le contrôle de la maladie.
Vectormune®ND est la solution pour le contrôle de la maladie de Newcastle chez la dinde.
Référence : Immunity Elicited by a Turkey Herpesvirus-Vectored Newcastle Disease Vaccine in Turkey Against Challenge With a Recent Genotype IV Newcastle Disease Virus Field Strain ; Abderrazak El Khantour,A Sami Darkaoui,B T´ımea Tata´r-Kis,C Tama´s Mato,´ C Amal Essalah-Bennani,D Christophe Cazaban,E and Vilmos Palya ; AVIAN DISEASES 61:378–386, 2017

 Corporate Website
Corporate Website
 Africa
Africa
 Argentina
Argentina
 Asia
Asia
 Australia
Australia
 Belgium
Belgium
 Brazil
Brazil
 Bulgaria
Bulgaria
 Canada (EN)
Canada (EN)
 Chile
Chile
 China
China
 Colombia
Colombia
 Denmark
Denmark
 Egypt
Egypt
 France
France
 Germany
Germany
 Greece
Greece
 Hungary
Hungary
 Indonesia
Indonesia
 Italia
Italia
 India
India
 Japan
Japan
 Korea
Korea
 Malaysia
Malaysia
 Mexico
Mexico
 Middle East
Middle East
 Netherlands
Netherlands
 Peru
Peru
 Philippines
Philippines
 Poland
Poland
 Portugal
Portugal
 Romania
Romania
 Russia
Russia
 South Africa
South Africa
 Spain
Spain
 Sweden
Sweden
 Thailand
Thailand
 Tunisia
Tunisia
 Turkey
Turkey
 Ukraine
Ukraine
 United Kingdom
United Kingdom
 USA
USA
 Vietnam
Vietnam